Korrosion ist allgegenwärtig, sie tritt in einer chemischen Fabrik, in der Küche und im Freien auf. Deswegen sind korrosionsbeständige Stähle sehr wichtig und haben einen sehr breiten Anwendungsbereich.
Dafür benötigen wir jedoch verschiedene Sorten, die an die realen korrosiven Beanspruchungen so weit möglich angepasst sind. Dabei muss unbedingt das Medium, in dem ein Stahl eingesetzt werden soll, beachtet werden. Einen universellen Stahl, der in jedem Medium korrosionsbeständig ist, gibt es leider nicht.
Ursache der Korrosionsbeständigkeit
Warum korrodieren diese Stähle nicht? Grundsätzlich unterscheiden wir bei Metallen zwei Wege zur Korrosionsbeständigkeit:
Einige Metalle (das Paradebeispiel ist Gold) reagieren mit Sauerstoff nicht, sind sozusagen von ihrer elektrochemischen Natur her beständig. Diese Metalle sind jedoch selten, teuer und wir können sie nicht breit verwenden.
Einige technische Metalle sind aus einem anderen Grund korrosionsbeständig. Sie bilden selbstständig eine schützende Schicht, die als Passivschicht bezeichnet wird.
Diese Metalle sind von Natur her sozusagen beschichtet. Eine Passivschicht entsteht durch eine Reaktion des Metalls mit Sauerstoff und sie ist viel besser, als viele Schichten, die wir oft auf Werkstoffe auftragen.
Passivschichten zeichnen sich dadurch aus, dass sie sehr dünn sind und sehr gut auf dem Metall haften. Das Gute ist auch, dass sie sich nach Verletzungen (z. B. zerkratzen mit einem Messer) selbst heilen. Zu diesen passivierbaren Metallen gehören die korrosionsbeständigen Stähle. Eine schützende Passivschicht entsteht bei Stählen, sofern bestimmte Voraussetzungen erfüllt sind.
Die wichtigste Voraussetzung ist, dass der Stahl mindestens 12 % Chrom, enthalten muss. Somit sind alle korrosionsbeständigen Stähle hochlegierte Chrom-Stähle. Chrom überträgt seine eigene Fähigkeit zum Passivieren auf Stahl. Die unsichtbare Passivschicht bildet sich selbstständig aus, ist 10 bis 30 nm dick, elektronenleitend und besteht aus Chromoxid.
Eine zweite Voraussetzung ist, dass das Chrom mit dem Eisen nur Mischkristalle bilden muss. Es dürfen keine Chromkarbide entstehen. Chrom neigt aber zur Karbidbildung. Daher müssen diese Stähle sehr wenig Kohlenstoff (weniger als 0,1 %, am besten max. 0,01 %) enthalten. Ein Zusatz anderer Legierungselemente (z. B. Titan), die Karbide bilden, kann ebenfalls hilfreich sein.
Häufig werden diesen Stählen weitere Legierungselemente zugesetzt, vor allem Nickel und Molybdän. Sie haben eine die Korrosionsbeständigkeit erhöhende Wirkung. Nickel begünstigt ein austenitisches Gefüge, Molybdän die Korrosionsbeständigkeit in chloridhaltigen Medien. Für die Sicherung der Korrosionsbeständigkeit sind hohe Reinheitsgrade der Stähle notwendig.
Die Erfüllung dieser Voraussetzungen ist nur durch eine aufwendige Herstellung möglich. Oft kommen spezielle Methoden, wie z. B. der VOD-Prozess (Vacuum Oxygen Decarburisation), zum Einsatz.
Bewertung der Korrosionsbeständigkeit
Für die Bewertung der Korrosionsbeständigkeit dieser Stähle wird in der Praxis der sog. PREN-Wert (Pitting–Resistance–Equivalent-Number) benutzt. Diese Bewertung wird insbesondere beim Einsatz in chlorhaltigen Medien angewandt.
Die Kennzahl wird nach einer bestimmten Regel berechnet. Je höher der PREn-Wert ist, desto besser die Korrosionsbeständigkeit des Stahls. Weitere Legierungselemente müssen dennoch beachtet werden. Aus Erfahrung wissen wir, dass erst Werte von 30 und höher die sichere langfristige Beständigkeit z. B. im Meerwasser bedeuten.
Die in Abb. 1a gezeigte Probe ist ein kleiner Beweis für die gute Korrosionsbeständigkeit dieser Stähle. Sie wurde etwa 30 Jahre der Nordsee-Atmosphäre auf Helgoland ausgesetzt. Weitere Informationen finden Sie unter Beständigkeit nichtrostender Stähle.
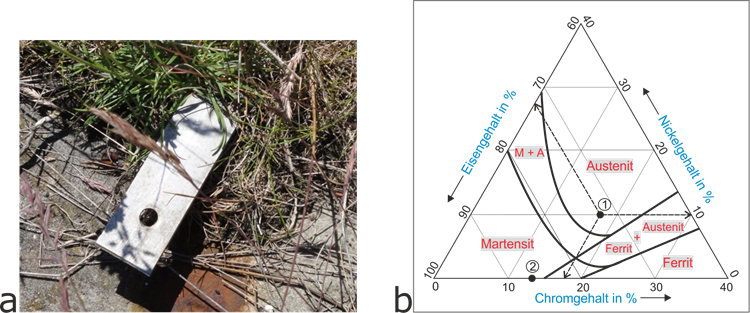 Abb. 1 Korrosionsbeständige Stähle a) Probe nach 30 Jahren auf Helgoland, b) Gefügeausbildung
Abb. 1 Korrosionsbeständige Stähle a) Probe nach 30 Jahren auf Helgoland, b) Gefügeausbildung
Einteilung der korrosionsbeständigen Stähle
Die Einteilung korrosionsbeständiger Stähle erfolgt nach ihrem Gefüge, das von der Zusammensetzung abhängig ist. Die Gefügeausbildung ist in Abb. 1b vereinfacht dargestellt.
Entscheidend sind die Anteile an Chrom und Nickel. Im Diagramm ist ein großes Austenit-Feld gut erkennbar und es bedeutet, dass ein austenitisches Gefüge auch bei einer Kombination der beiden Elemente Chrom und Nickel entsteht. Das geschieht auch, wenn Nickel als Austenitbildner in einem geringeren Anteil als Chrom (ein Ferritbildner) vorhanden ist.
Diese Erkenntnis ist wichtig, da Nickel zu den teuren Metallen gehört und jede Möglichkeit den Nickelgehalt zu erniedrigen, von wirtschaftlicher Bedeutung ist. Nehmen wir beispielsweise den Punkt 1. Er entspricht der Stahlzusammensetzung von 18 % Chrom und 10 % Nickel und liegt im Austenit-Feld.
Dem Diagramm entnehmen wir auch weitere mögliche Zusammensetzungen, die zu anderen Gefüge führen. Dabei müssen die Chromgehalte – wegen der Ausbildung der Passivschicht – stets rechts vom Punkt 2 (12 % Chrom) liegen.
Entsprechend der möglichen Gefügeausbildung werden folgende vier Gruppen korrosionsbeständiger Stähle unterschieden: ferritische Stähle (Ferrite), austenitische Stähle (Austenite), austenitisch-ferritische Stähle (Duplex-Stähle) und martensitische Stähle.
Ferritische, austenitische und ferritisch-austenitische Stähle haben sehr wenig Kohlenstoff und sind dadurch umwandlungsfrei, d. h. bei Temperaturänderungen findet keine Gitterumwandlung von Eisen (s. Eigenschaften von Eisen) statt. Diese Stähle haben fast im gesamten Temperaturbereich das durch die Zusammensetzung bedingte Gefüge. Somit sind das Härten und alle mit dem Härten verbundenen Wärmebehandlungen (z. B. Vergüten) dieser Stähle nicht möglich.
Martensitische Stähle besitzen dagegen mehr Kohlenstoff. Dadurch sind sie umwandlungsfähig und zum Härten geeignet. Durch den erhöhten Kohlenstoffgehalt wird die Korrosionsbeständigkeit jedoch vermindert und Bauteile oder Gegenstände aus diesen Stählen müssen poliert werden.
Ferritische, austenitische und ferritisch-austenitische Stähle werden im Anlieferungszustand verwendet.
Martensitische Stähle werden (als Bauteile) dagegen erst nach einem geeigneten Härten verwendet.
Das hier dargestellte Diagramm zur Gefügeausbildung (Abb. 1b) ist zwar anschaulich, aber für praktische Zwecke zu ungenau. In der Praxis bedienen sich die Fachleute mit dem genauen Schaeffler-Diagramm, das ständig verbessert und erweitert wird. Bei diesem Diagramm werden sog. Chrom- und Nickel- Equivalente betrachtet, mit denen mehre Ferrit- bzw. Austenitbildner berücksichtigt werden.
Benennung korrosionsbeständiger Stähle
Korrosionsbeständige Stähle werden unterschiedlich bezeichnet und oft tragen sie Handelsnamen.
Zum Beispiel als Edelstahl Rostfrei in Deutschland (alleine „Edelstahl“ bedeutet Stahlsorten mit besonders hoher Reinheit, die nicht zwangsläufig hochlegiert und rostfrei sind) oder als Inox-Stahl in Frankreich.
„Cromargan“ ist der Handelsname vom WMF, „Nirosta“ ist Markenname von ThyssenKrupp Stainless.
Sehr verbreitet ist auch die alte Bezeichnung „VA-Stahl“ (V2A, V4A). Sie ist 1912 bei der Entwicklung der ersten Stähle entstanden. Mit „V“ hat man damals eine Versuchsschmelze markiert und „A“ bedeutete Austenit. Bis heute sind diese kurzen und bequemen Bezeichnungen im Einsatz.
Anwendung der korrosionsbeständigen Stähle
Korrosionsbeständige Stähle sind für den Einsatz unter korrosiven Bedingungen vorgesehen. Bei der Auswahl eines für ein bestimmtes Medium geeigneten Stahls müssen immer die Einsatzbedingungen beachtet werden. Bedingt durch unterschiedliche Zusammensetzungen und Gefüge unterscheiden sich die korrosionsbeständigen Stähle in ihren Eigenschaften und so können sie in verschiedenen Bereichen verwendet werden.
Ihre Anwendung gehört zu den breitesten in der ganzen Werkstoffkunde: von der Küche bis zur chemischen Industrie, von Rasiermessern und Besteck bis zu Turbinenschaufeln und Laufrädern. Diese hochwertigen Stähle verwenden wir im Bauwesen (Fassaden), im Schiffbau (Tanks), im Maschinenbau, in der Uhrentechnik, in der Medizintechnik und anderen Bereichen wie Lebensmittelindustrie, Waschmaschinen und Geschirrspüler, Abgassysteme, Wärmetauscher, Meerwasserentsalzungsanlagen.
Abb. 2 zeigt nur zwei kleine Beispiele dieser vielfältigen Anwendungen. Abb. 2 Anwendungsbeispiele für Edelstähle a) Auf einem Schiff, b) Kochtopf
Abb. 2 Anwendungsbeispiele für Edelstähle a) Auf einem Schiff, b) Kochtopf
Edelstahltöpfe und Salzen von Speisen
Zum Schluss ein besonderes Thema. Es wird oft darauf hingewiesen, dass wir Salz immer erst beim kochenden Wasser in einen Edelstahltopf einrühren sollen. Haben Sie das schon gewusst? Jeder Italiener würde dies sagen, wenn wir mit ihm über Kochen von Spagetti sprechen.
Aber warum sollen wir so vorgehen? Hat es etwas mit Spagetti zu tun? Nein, diese Forderung hängt mit Passivschicht zusammen, die für die Korrosionsbeständigkeit des Edelstahltopfes verantwortlich sind.
Die Schicht hat nämlich eine Schwäche: Sie kann von bestimmten Stoffen (in Form von Ionen) angegriffen werden und dann schützt sie das Metall schlechter. Der Feind austenitischer korrosionsbeständiger Stähle heißt Chlorid-Ion. Das Kochsalz enthält diese gefährlichen Ionen, die bei Auflösen des Salzes in Wasser frei werden. Die Ionen – kleine und elektrisch geladenen Teilchen – können die Passivschicht durchbrechen und so an das „nackte“ Metall gelangen. Das Metall beginnt dann zu korrodieren.
Für Kochtöpfe (Abb 2b) wird meist der Stahl „18/10“ verwendet. Er ist ein der einfachsten aus der austenitischen Gruppe und seine Passivschicht ist besonders bei Chloriden anfällig. Bei kaltem Wasser löst sich das Kochsalz viel langsamer und somit liegen Salzteilchen am Topfboden, aus denen die Ionen entweichen können. Beim kochenden Wasser löst sich das Salz sehr schnell, keine Salzpartikel liegen am Topfboden und die Chlorid-Ionen können keinen großen Schaden einrichten. <<





